中国医疗器械注册技术服务与代办
一、为什么医疗器械需要注册?
根据中华人民共和国国家食品药品监督管理总局在2014年7月30日办法的第4号令《医疗器械注册管理办法》中,第二条规定如下:在中华人民共和国境内销售、使用的医疗器械,应当按照本办法的规定申请注册或者办理备案。
具体内容参加如下链接http://www.sda.gov.cn/WS01/CL0053/103756.html
二、我的产品需要做医疗器械注册吗?
以下为医疗器械分类目录,如果你的产品在这个目录内,那就必须要做医疗器械注册了。

三、医疗器械注册法规条例
1、《医疗器械监督管理条例》(国务院令第650号)2014年03月07日 发布 [1]
2、《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)2014年07月30日 发布 [2]
3、《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)2014年07月30日 发布
四、医疗器械注册-监管模式
在我国,第二类、第三类医疗器械实行注册管理。
境内第一类医疗器械备案,备案人向设区的市级食品药品监督管理部门提交备案资料。
境内第二类医疗器械由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。
境内第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
进口第一类医疗器械备案,备案人向国家食品药品监督管理总局提交备案资料。
进口第二类、第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
香港、澳门、台湾地区医疗器械的注册、备案,参照进口医疗器械办理。
五、医疗器械注册需要的资料:
1、 申请表;
2、 证明性文件;
3、 医疗器械安全有效基本要求清单;
4、 综述资料;
5、 研究资料;
6、 生产制造信息;
7、 临床评价资料;
8、 产品风险分析资料;
9、 产品技术要求;
10、 产品注册检验报告;
11、 产品说明书;
12、 最小销售单元的标签样稿;
13、 符合性声明及自我保证声明;
14、 企业认为需要申报的其他文件资料。
这么多资料你是不是看不懂了,不知道需要什么资料?没关系有我们在,你都可以轻松搞定。请参考第四条。
六、医疗器械注册-我们能为你做什么?
上海
世复检测技术服务有限公司在医疗器械注册领域有着很多成功经验:无论是国产、进口无论是有源、无源,无论是有菌、无菌,我们统统可以帮您轻松搞定。
我们的工程师都是一直游走于行业最前沿,掌握了最新的知识法规,积累的最多的人脉和资源。
如果你还在为注册医疗器械而苦恼,那么请与我们联系,我们提供一站式服务。
七、医疗器械注册流程
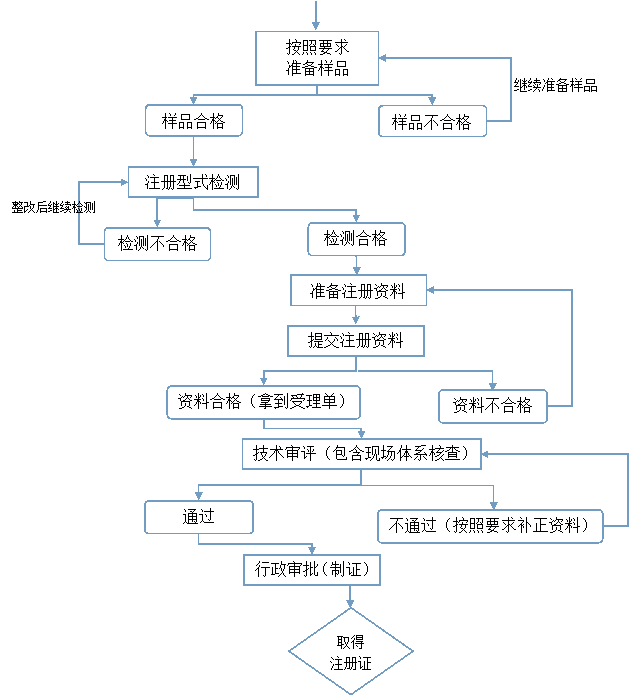
上海世复检测以丰富医疗器械注册 行业经验,专业办理一类,二类三类医疗器械注册技术服务,流程短,时间快,费用低。
服务热线:021-65667889/13386062867